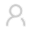10月8日,民众在比利时布鲁塞尔的一个新冠病毒检测点门口了解信息
10月8日,民众在比利时布鲁塞尔的一个新冠病毒检测点门口了解信息欧美多个国家正努力遏制“第二波疫情”扩散。为加速筛查病例,不少国家扩大使用更快速廉价的新冠抗原检测手段,以克服核酸检测能力不足的瓶颈。
但科学界提醒,抗原检测不如核酸检测准确率高,只能作为后者补充。
急需提速 上周全球新增200万例
路透社报道,德国13日新增新冠确诊病例4122例,累计确诊病例近33万例。新冠抗原检测可在几分钟内出结果,单次检测费5.9欧元(约合47元人民币)。德国目前每月可做900万次抗原检测,理论上可覆盖10%以上人口。
德国罗伯特·科赫研究所建议把抗原检测作为现有聚合酶链式反应(PCR)检测、即核酸检测的补充。
科学界将PCR检测结果作为诊断人体是否感染新冠病毒的主要标准,但不少国家核酸检测量不足,原因是实验室检测能力赶不上疫情扩散速度,检测试剂需求量也超过制造商生产能力。
德国亥姆霍兹传染研究中心流行病部门主任格拉尔德·克劳泽说,扩大抗原检测可能大大改变这种困境:可鼓励无症状者接受抗原检测,把核酸检测留给那些出现疑似新冠症状的病人。
全球新冠病毒感染人数仍在急剧攀升。据世界卫生组织报告,上周全球新增新冠病例超过200万例,累计确诊病例约3700万例,累计病亡病例超过100万例。如今冬季流感季即将来临,多国卫生部门急需扩充检测手段以加速病例筛查。意大利、美国和加拿大也已购买数以百万计抗原检测试剂。
需求量大 法国每周检测超百万人次
一些国家新冠疫情扩散较快,依照现有检测手段,卫生部门难以迅速、全面追踪病毒感染路径。
路透社报道,美国整个夏季依赖自动化PCR检测机器筛查病例,让不少病人苦等检测结果超过一周。欧洲新冠病毒检测同样有缺陷。
法国为民众免费提供新冠病毒检测,每周检测量逾百万人次,但民众需排长队等候接受检测和获取结果。研究机构后续推出据说能在40分钟内出结果、无需拭子的检测工具。
意大利卫生部称,该国目前每周可做80万至84万次新冠病毒检测,是4月时的两倍多。然而,政府抗疫顾问、帕多瓦大学微生物学教授安德烈亚·克里桑蒂说,要控制住疫情蔓延速度,意大利每周检测量需达200万次。
荷兰是欧洲新冠感染率最高的国家之一,正努力提高检测能力,目标是下周把操作检测和实验室处理检测样本的数量从现在的28万份提高到38.5万份,12月则达到每周近50万份。
应作“替补” 抗原检测“假阴性”概率高
瑞士罗氏(制药)公司13日宣布,今年年底前推出新的抗原检测工具,由实验室设备操作,不算样本采集时间,每小时最多可处理300份检测样本。罗氏称,到2021年初,这种检测试剂每月产量大约5000万份,超过该公司目前在售即时检测产品。
对比PCR检测,抗原检测快捷、廉价,但出现“假阴性”结果的概率更高,因而一些专家建议,只有在没有其他选择的情况下使用抗原检测。各国就如何应用抗原检测的立场不断变化。
瑞士单日新增病例6月时一度呈个位数,如今飙升至大约1500例,刚开始验证快速抗原检测的准确性。
“在适当领域应用快速检测将融入我们的检测战略,”瑞士卫生部一名发言人说,“我们将在11月更新检测建议。”
德国法兰克福大学医院医学病毒学研究所主任桑德拉·齐泽克说,前往养老院探望老人的无症状人员可选择做快速抗原检测,但不应当把它视为新冠感染诊断的最权威手段。
“PCR检测依然是黄金标准,”齐泽克说,“抗原检测应当只用作无法及时做PCR检测情况下的一种替代手段。”
延伸
美国礼来公司暂停新冠防治临床试验
美国制药企业礼来公司13日宣布,出于“安全考虑”,暂停一项新冠抗体疗法三期临床试验。
这是继英国阿斯利康制药、美国强生公司后,第三家大型制药企业因相似原因暂停新冠疫苗或抗体疗法临床试验。
礼来公司发言人莫莉·麦卡利在一份邮件声明中说,“出于极度谨慎”,一个独立的数据安全监测委员会建议停止试验,“礼来支持这一决定”。
这家药企没有披露任何关联“安全考虑”的试验细节。暂时不清楚这一试验暂停是否影响礼来关联新冠病毒的其他临床试验项目。
礼来8月3日宣布启动抗体疗法三期临床试验ACTIV-3,主要研究LY-CoV555抗体能否有效预防新冠病毒感染等。这一抗体由礼来与总部位于加拿大温哥华的生物技术企业AbCellera共同研发。
礼来说,LY-CoV555抗体是一种针对新冠病毒刺突蛋白的单克隆抗体,从美国一名早期康复患者的血液样本中分离而来。它能阻止病毒附着和进入人体细胞,有望用于预防和治疗新冠病毒感染。
ACTIV-3项目主要试验地点位于美国,另一些在丹麦和新加坡,目标是召集1万名确诊患者,分为两组作观察:试验组接受礼来公司的抗体疗法,同时服用抗病毒药物瑞德西韦;对照组仅服用瑞德西韦。
ACTIV-3试验获得美国国家卫生研究院支持。本月早些时候,礼来依据另外一项临床数据的数据,向美国食品和药物管理局申请LY-CoV555抗体的紧急使用授权,用于治疗轻中症患者。
多家媒体报道,新冠抗体疗法因美国总统唐纳德·特朗普的“宣传”名声大噪。
特朗普2日凌晨宣布他和妻子梅拉尼娅的新冠病毒检测结果呈阳性,随后进入马里兰州沃尔特·里德国家军事医疗中心接受治疗,5日出院返回白宫,继续接受全天医疗护理,11日自称完全康复。
白宫医生说,特朗普接受的是美国再生元制药公司的“抗体鸡尾酒疗法”以及瑞德西韦治疗。特朗普本人多次称赞抗体疗法。不过,再生元制药的“抗体鸡尾酒疗法”尚未获得美国药管局使用授权。
礼来宣布暂停临床试验前一天,强生宣布,暂停旗下杨森制药公司在研新冠疫苗的临床试验,原因是一名受试者出现“无法解释的疾病”。
按照强生的说法,试验只是“暂时停止”,大型试验出现受试者生病等情况并不罕见;某些情况下,出现疾病可能与试验仅有部分关联或完全无关。
不过,一个独立委员会审查完疫苗相关数据后,阿斯利康9月12日说,疫苗安全性获得英国独立委员会和监管机构认可。这款疫苗在英国、巴西、南非和印度的临床试验随后相继恢复,但在美国的试验依然暂停。
本组文并图/新华社